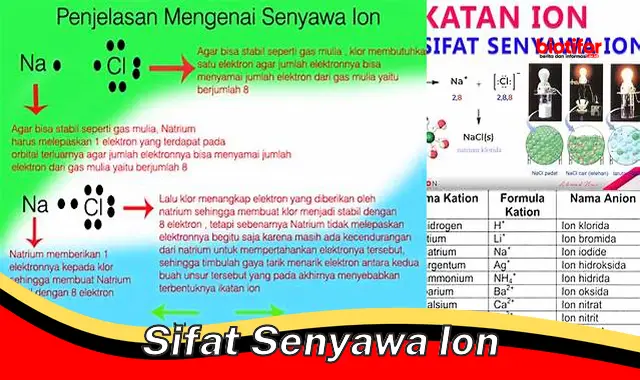
Sifat senyawa ion adalah senyawa yang terbentuk dari ion-ion yang berlawanan muatan. Ion adalah atom atau molekul yang memiliki muatan listrik karena kelebihan atau kekurangan elektron. Senyawa ion umumnya memiliki titik leleh dan titik didih yang tinggi, serta dapat larut dalam air. Contoh senyawa ion adalah natrium klorida (NaCl), kalium bromida (KBr), dan kalsium oksida (CaO).
Senyawa ion memiliki beberapa sifat penting, antara lain:
- Titik leleh dan titik didih yang tinggi
- Kelarutan yang tinggi dalam air
- Daya hantar listrik yang baik
Sifat-sifat ini membuat senyawa ion banyak digunakan dalam berbagai aplikasi, seperti:
- Sebagai elektrolit dalam baterai dan sel bahan bakar
- Sebagai bahan baku pembuatan kaca dan keramik
- Sebagai pupuk dalam pertanian
Senyawa ion memiliki sejarah panjang dalam kimia. Senyawa ion pertama kali diidentifikasi oleh Antoine Lavoisier pada tahun 1789. Sejak saat itu, senyawa ion telah menjadi salah satu jenis senyawa kimia yang paling banyak dipelajari dan digunakan.
sifat senyawa ion
Sifat senyawa ion merujuk pada karakteristik khas senyawa yang terbentuk dari ion-ion yang berlawanan muatan. Sifat-sifat ini menentukan perilaku dan aplikasi senyawa ion dalam berbagai bidang.
- Titik leleh tinggi
- Titik didih tinggi
- Kelarutan tinggi dalam air
- Penghantar listrik yang baik
- Bentuk kristal yang khas
- Reaktivitas kimia yang tinggi
- Kegunaan yang luas
- Peran penting dalam sistem biologis
Sifat-sifat ini saling terkait dan berkontribusi pada peran penting senyawa ion dalam berbagai bidang, seperti industri, teknologi, dan biologi. Misalnya, titik leleh dan titik didih yang tinggi membuat senyawa ion cocok digunakan sebagai bahan tahan api dan keramik. Kelarutannya yang tinggi dalam air memungkinkan senyawa ion digunakan sebagai elektrolit dalam baterai dan sel bahan bakar.
Titik leleh tinggi
Titik leleh tinggi merupakan salah satu sifat penting senyawa ion. Titik leleh adalah suhu di mana suatu zat berubah dari fase padat ke fase cair. Senyawa ion memiliki titik leleh yang tinggi karena adanya gaya tarik elektrostatik yang kuat antara ion-ion penyusunnya. Gaya tarik ini membutuhkan energi yang besar untuk diatasi, sehingga senyawa ion sulit untuk dilelehkan.
-
Kisi Kristal yang Kuat
Senyawa ion tersusun dalam kisi kristal yang teratur, di mana ion-ion positif dan negatif tersusun secara berselang-seling. Kisi kristal ini sangat kuat dan membutuhkan energi yang besar untuk dipecah, sehingga titik leleh senyawa ion menjadi tinggi.
-
Muatan Ion yang Besar
Senyawa ion umumnya terdiri dari ion-ion dengan muatan yang besar, seperti +2 atau -2. Muatan yang besar ini menghasilkan gaya tarik elektrostatik yang lebih kuat, sehingga titik leleh senyawa ion menjadi lebih tinggi.
-
Ukuran Ion yang Kecil
Senyawa ion umumnya terdiri dari ion-ion dengan ukuran yang kecil, seperti ion natrium (Na+) dan ion klorida (Cl-). Ukuran ion yang kecil memungkinkan ion-ion untuk saling mendekati dan membentuk kisi kristal yang lebih rapat, sehingga titik leleh senyawa ion menjadi lebih tinggi.
-
Aplikasi Titik Leleh Tinggi
Titik leleh tinggi senyawa ion menjadikannya bahan yang cocok untuk berbagai aplikasi, seperti:
- Bahan tahan api: Senyawa ion dengan titik leleh tinggi dapat digunakan sebagai bahan tahan api dalam tungku dan industri lainnya.
- Bahan keramik: Senyawa ion dengan titik leleh tinggi juga banyak digunakan sebagai bahan pembuat keramik.
Dengan demikian, titik leleh tinggi merupakan salah satu sifat penting senyawa ion yang menentukan banyak aplikasinya dalam berbagai bidang industri dan teknologi.
Titik didih tinggi
Titik didih merupakan suhu di mana tekanan uap suatu zat sama dengan tekanan lingkungan, sehingga zat tersebut berubah dari fase cair ke fase gas. Senyawa ion umumnya memiliki titik didih yang tinggi karena adanya gaya tarik elektrostatik yang kuat antara ion-ion penyusunnya. Gaya tarik ini membutuhkan energi yang besar untuk diatasi, sehingga senyawa ion sulit untuk diuapkan.
-
Kisi Kristal yang Kuat
Senyawa ion tersusun dalam kisi kristal yang teratur, di mana ion-ion positif dan negatif tersusun secara berselang-seling. Kisi kristal ini sangat kuat dan membutuhkan energi yang besar untuk dipecah, sehingga titik didih senyawa ion menjadi tinggi.
-
Muatan Ion yang Besar
Senyawa ion umumnya terdiri dari ion-ion dengan muatan yang besar, seperti +2 atau -2. Muatan yang besar ini menghasilkan gaya tarik elektrostatik yang lebih kuat, sehingga titik didih senyawa ion menjadi lebih tinggi.
-
Ukuran Ion yang Kecil
Senyawa ion umumnya terdiri dari ion-ion dengan ukuran yang kecil, seperti ion natrium (Na+) dan ion klorida (Cl-). Ukuran ion yang kecil memungkinkan ion-ion untuk saling mendekati dan membentuk kisi kristal yang lebih rapat, sehingga titik didih senyawa ion menjadi lebih tinggi.
-
Aplikasi Titik Didih Tinggi
Titik didih tinggi senyawa ion menjadikannya bahan yang cocok untuk berbagai aplikasi, seperti:
- Bahan pelarut: Senyawa ion dengan titik didih tinggi dapat digunakan sebagai pelarut untuk reaksi kimia yang membutuhkan suhu tinggi.
- Bahan pengering: Senyawa ion dengan titik didih tinggi dapat digunakan sebagai bahan pengering karena sifatnya yang tidak mudah menguap.
Dengan demikian, titik didih tinggi merupakan salah satu sifat penting senyawa ion yang menentukan banyak aplikasinya dalam berbagai bidang industri dan teknologi.
Kelarutan tinggi dalam air
Kelarutan tinggi dalam air merupakan salah satu sifat penting senyawa ion. Kelarutan suatu zat dalam air ditentukan oleh kemampuan zat tersebut untuk berinteraksi dengan molekul air. Senyawa ion memiliki kelarutan tinggi dalam air karena ion-ion penyusunnya dapat berinteraksi dengan molekul air melalui gaya tarik elektrostatik.
Gaya tarik elektrostatik antara ion dan molekul air terjadi karena molekul air memiliki kutub positif dan negatif. Kutub positif molekul air tertarik pada ion negatif, sedangkan kutub negatif molekul air tertarik pada ion positif. Interaksi ini membentuk ikatan ion-dipol, yang memungkinkan senyawa ion larut dalam air.
Kelarutan tinggi dalam air senyawa ion menjadikannya bahan yang penting dalam berbagai aplikasi, seperti:
-
Elektrolit
Senyawa ion yang larut dalam air dapat membentuk larutan elektrolit. Larutan elektrolit dapat menghantarkan listrik karena ion-ion yang terlarut dapat bergerak bebas dalam larutan. Elektrolit digunakan dalam berbagai aplikasi, seperti baterai, sel bahan bakar, dan elektroplating.
-
Pupuk
Senyawa ion yang larut dalam air banyak digunakan sebagai pupuk dalam pertanian. Pupuk ini menyediakan ion-ion penting yang dibutuhkan tanaman untuk tumbuh dan berkembang.
-
Bahan pembersih
Senyawa ion yang larut dalam air juga digunakan sebagai bahan pembersih. Bahan pembersih ini dapat melarutkan kotoran dan noda karena ion-ion yang terlarut dapat berinteraksi dengan molekul kotoran dan noda.
Dengan demikian, kelarutan tinggi dalam air merupakan salah satu sifat penting senyawa ion yang menentukan banyak aplikasinya dalam berbagai bidang industri, pertanian, dan rumah tangga.
Penghantar Listrik yang Baik
Sifat penghantar listrik yang baik merupakan salah satu sifat penting senyawa ion. Penghantar listrik adalah bahan yang dapat menghantarkan arus listrik. Senyawa ion dapat menghantarkan listrik karena ion-ion penyusunnya dapat bergerak bebas dalam larutan atau lelehan.
-
Ion Sebagai Pembawa Muatan
Ion adalah partikel bermuatan, yang dapat bermuatan positif atau negatif. Ketika senyawa ion dilarutkan dalam air atau dilelehkan, ion-ion ini terpisah dan dapat bergerak bebas. Gerakan ion-ion ini memungkinkan terjadinya aliran listrik.
-
Konsentrasi Ion
Penghantaran listrik senyawa ion dipengaruhi oleh konsentrasi ion dalam larutan atau lelehan. Semakin tinggi konsentrasi ion, semakin banyak pembawa muatan yang tersedia dan semakin baik kemampuan penghantaran listrik.
-
Aplikasi Penghantar Listrik
Sifat penghantar listrik yang baik senyawa ion menjadikannya bahan yang penting dalam berbagai aplikasi, seperti:
- Elektrolit dalam baterai dan sel bahan bakar
- Konduktor dalam kabel dan perangkat elektronik
- Sensor dan elektroda dalam peralatan analitik
Dengan demikian, sifat penghantar listrik yang baik senyawa ion sangat penting dalam berbagai aplikasi industri dan teknologi. Sifat ini memungkinkan senyawa ion digunakan sebagai bahan untuk menghantarkan arus listrik, menyimpan energi, dan mendeteksi berbagai zat.
Bentuk kristal yang khas
Bentuk kristal yang khas merupakan salah satu sifat penting senyawa ion. Senyawa ion cenderung membentuk kristal dengan bentuk yang teratur dan simetris karena susunan ion-ion penyusunnya yang teratur dalam kisi kristal. Bentuk kristal ini mencerminkan sifat kimia dan ikatan dalam senyawa ion.
-
Struktur Kisi Kristal
Bentuk kristal senyawa ion ditentukan oleh struktur kisi kristalnya. Kisi kristal merupakan susunan ion-ion positif dan negatif yang teratur dan berulang. Struktur kisi kristal yang umum pada senyawa ion antara lain kisi kubus sederhana, kisi kubus berpusat muka, dan kisi heksagonal rapat. Struktur kisi kristal ini menentukan bentuk kristal yang khas untuk setiap senyawa ion.
-
Jenis Ion
Jenis ion penyusun juga memengaruhi bentuk kristal senyawa ion. Senyawa ion yang terdiri dari ion-ion dengan ukuran dan muatan yang sama cenderung membentuk kristal dengan bentuk yang lebih sederhana, seperti kubus atau oktahedron. Sebaliknya, senyawa ion yang terdiri dari ion-ion dengan ukuran dan muatan yang berbeda cenderung membentuk kristal dengan bentuk yang lebih kompleks.
-
Contoh Bentuk Kristal Senyawa Ion
Beberapa contoh bentuk kristal senyawa ion yang khas antara lain:
- Natrium klorida (NaCl): Kubus
- Kalium bromida (KBr): Kubus berpusat muka
- Kalsium fluorida (CaF2): Oktahedron
-
Aplikasi Bentuk Kristal Senyawa Ion
Bentuk kristal yang khas senyawa ion memiliki berbagai aplikasi, seperti:
- Identifikasi senyawa ion: Bentuk kristal dapat digunakan untuk mengidentifikasi senyawa ion tertentu.
- Pembuatan bahan: Senyawa ion dengan bentuk kristal tertentu dapat digunakan untuk membuat bahan dengan sifat yang diinginkan, seperti keramik dan semikonduktor.
Bentuk kristal yang khas merupakan salah satu sifat penting senyawa ion yang mencerminkan sifat kimia dan ikatan dalam senyawa tersebut. Bentuk kristal ini memiliki berbagai aplikasi dalam berbagai bidang, termasuk identifikasi senyawa ion dan pembuatan bahan.
Reaktivitas Kimia yang Tinggi
Senyawa ion memiliki reaktivitas kimia yang tinggi karena adanya ion-ion yang berlawanan muatan yang membentuknya. Ion-ion ini sangat reaktif dan cenderung bereaksi dengan zat lain untuk membentuk senyawa yang lebih stabil.
-
Reaksi dengan Logam
Senyawa ion dapat bereaksi dengan logam untuk membentuk senyawa ion baru. Misalnya, natrium klorida (NaCl) dapat bereaksi dengan logam natrium (Na) untuk membentuk natrium klorida (Na2Cl).
-
Reaksi dengan Non-Logam
Senyawa ion juga dapat bereaksi dengan non-logam untuk membentuk senyawa ion baru. Misalnya, natrium klorida (NaCl) dapat bereaksi dengan gas klorin (Cl2) untuk membentuk natrium hipoklorit (NaClO).
-
Reaksi dengan Air
Senyawa ion dapat bereaksi dengan air untuk membentuk senyawa baru. Misalnya, natrium klorida (NaCl) dapat bereaksi dengan air untuk membentuk natrium hidroksida (NaOH) dan asam klorida (HCl).
-
Reaksi Pengendapan
Senyawa ion dapat bereaksi satu sama lain untuk membentuk senyawa ion baru yang tidak larut dalam air. Reaksi ini disebut reaksi pengendapan. Misalnya, natrium klorida (NaCl) dapat bereaksi dengan perak nitrat (AgNO3) untuk membentuk perak klorida (AgCl) yang tidak larut dalam air.
Reaktivitas kimia yang tinggi senyawa ion menjadikannya bahan yang penting dalam berbagai aplikasi, seperti:
- Produksi bahan kimia
- Pembuatan obat-obatan
- Pengolahan air
- Pembuatan baterai
- Pembuatan pupuk
Dengan demikian, reaktivitas kimia yang tinggi merupakan salah satu sifat penting senyawa ion yang menentukan banyak aplikasinya dalam berbagai bidang industri dan teknologi.
Kegunaan yang luas
Sifat-sifat unik senyawa ion, seperti titik leleh dan titik didih yang tinggi, kelarutan tinggi dalam air, daya hantar listrik yang baik, bentuk kristal yang khas, reaktivitas kimia yang tinggi, menjadikannya bahan yang sangat berguna dalam berbagai bidang.
-
Bahan Bangunan
Senyawa ion seperti semen (kalsium silikat hidrat) dan gipsum (kalsium sulfat dihidrat) digunakan sebagai bahan bangunan karena kekuatan dan daya tahannya.
-
Pupuk
Senyawa ion seperti amonium nitrat dan kalium fosfat banyak digunakan sebagai pupuk untuk meningkatkan hasil pertanian.
-
Bahan Pembersih
Senyawa ion seperti natrium klorida dan natrium karbonat digunakan sebagai bahan pembersih karena kemampuannya menghilangkan kotoran dan noda.
-
Bahan Obat-obatan
Senyawa ion seperti natrium klorida dan kalium klorida digunakan dalam larutan infus dan obat-obatan lainnya.
Kegunaan senyawa ion yang luas ini sangat penting bagi kehidupan modern, berkontribusi pada infrastruktur, pertanian, kebersihan, dan kesehatan. Sifat-sifat unik senyawa ion menjadikannya bahan yang sangat berharga dalam berbagai aplikasi, mulai dari konstruksi hingga perawatan kesehatan.
Peran penting dalam sistem biologis
Senyawa ion memainkan peran penting dalam sistem biologis karena sifat uniknya, seperti kelarutannya yang tinggi dalam air dan kemampuannya untuk menghantarkan listrik. Sifat-sifat ini memungkinkan senyawa ion untuk berpartisipasi dalam berbagai proses biologis yang penting.
Salah satu peran penting senyawa ion dalam sistem biologis adalah sebagai elektrolit. Elektrolit adalah zat yang dapat menghantarkan listrik karena mengandung ion-ion yang dapat bergerak bebas. Dalam tubuh, elektrolit seperti natrium, kalium, dan klorida membantu mengatur keseimbangan cairan, tekanan osmotik, dan fungsi otot dan saraf.
Senyawa ion juga berperan penting dalam menjaga pH tubuh. pH adalah ukuran keasaman atau kebasaan suatu larutan, dan sangat penting untuk berfungsinya banyak proses biologis. Senyawa ion seperti bikarbonat dan fosfat bertindak sebagai buffer, membantu menjaga pH tubuh dalam kisaran yang sempit.
Selain itu, senyawa ion juga terlibat dalam banyak reaksi kimia yang penting untuk kehidupan. Misalnya, ion kalsium sangat penting untuk pembekuan darah dan kontraksi otot. Ion magnesium berperan dalam aktivitas enzim dan pembentukan tulang.
Memahami peran penting senyawa ion dalam sistem biologis sangat penting untuk menghargai kompleksitas dan keterkaitan kehidupan. Sifat-sifat unik senyawa ion memungkinkan mereka untuk berpartisipasi dalam berbagai proses biologis yang penting, mulai dari pengaturan keseimbangan cairan hingga pensinyalan saraf.
Serba-Serbi Senyawa Ion
Senyawa ion merupakan senyawa yang terbentuk dari ion-ion yang berlawanan muatan. Sifat-sifat unik senyawa ion, seperti titik leleh dan titik didih yang tinggi, kelarutan yang tinggi dalam air, daya hantar listrik yang baik, dan reaktivitas kimia yang tinggi, menjadikannya bahan yang sangat berguna dalam berbagai bidang. Berikut adalah beberapa pertanyaan umum dan jawabannya mengenai senyawa ion:
Pertanyaan 1: Apa itu senyawa ion?
Senyawa ion adalah senyawa yang terbentuk dari ion-ion yang berlawanan muatan. Ion adalah atom atau molekul yang memiliki muatan listrik karena kelebihan atau kekurangan elektron.
Pertanyaan 2: Apa saja sifat-sifat senyawa ion?
Sifat-sifat senyawa ion antara lain: titik leleh dan titik didih yang tinggi, kelarutan tinggi dalam air, daya hantar listrik yang baik, bentuk kristal yang khas, dan reaktivitas kimia yang tinggi.
Pertanyaan 3: Apa saja kegunaan senyawa ion?
Senyawa ion memiliki kegunaan yang luas, antara lain sebagai bahan bangunan, pupuk, bahan pembersih, bahan obat-obatan, dan elektrolit dalam baterai.
Pertanyaan 4: Apa peran senyawa ion dalam sistem biologis?
Senyawa ion memainkan peran penting dalam sistem biologis, antara lain sebagai elektrolit, pengatur pH, dan kofaktor dalam reaksi enzimatik.
Pertanyaan 5: Bagaimana cara mengidentifikasi senyawa ion?
Senyawa ion umumnya memiliki titik leleh dan titik didih yang tinggi, serta dapat larut dalam air. Selain itu, senyawa ion biasanya membentuk kristal dengan bentuk yang teratur.
Pertanyaan 6: Apa saja contoh senyawa ion?
Contoh senyawa ion antara lain natrium klorida (garam dapur), kalium bromida, kalsium oksida, dan magnesium sulfat.
Dengan memahami sifat-sifat dan kegunaan senyawa ion, kita dapat mengapresiasi peran pentingnya dalam berbagai bidang, mulai dari industri hingga kesehatan.
Baca terus untuk mengetahui lebih lanjut tentang senyawa ion dan aplikasinya dalam kehidupan kita sehari-hari.
Tips Memahami Sifat Senyawa Ion
Senyawa ion merupakan senyawa yang memiliki sifat-sifat unik dan penting dalam berbagai bidang. Berikut adalah beberapa tips untuk membantu Anda memahami sifat senyawa ion dengan lebih baik:
Tip 1: Pahami Konsep Ion
Sebelum mempelajari senyawa ion, penting untuk memahami konsep ion. Ion adalah atom atau molekul yang memiliki muatan listrik karena kelebihan atau kekurangan elektron. Muatan listrik inilah yang menyebabkan ion berinteraksi satu sama lain dan membentuk senyawa ion.
Tip 2: Ketahui Jenis-Jenis Ikatan Ion
Senyawa ion terbentuk melalui ikatan ion, yaitu ikatan yang terjadi antara ion positif (kation) dan ion negatif (anion). Sifat-sifat senyawa ion sangat dipengaruhi oleh jenis dan kekuatan ikatan ion yang terbentuk.
Tip 3: Perhatikan Ukuran dan Muatan Ion
Ukuran dan muatan ion penyusun sangat memengaruhi sifat-sifat senyawa ion. Ion dengan ukuran kecil dan muatan besar cenderung membentuk ikatan ion yang kuat dan menghasilkan senyawa ion dengan titik leleh dan titik didih yang tinggi.
Tip 4: Pelajari Kelarutan Senyawa Ion
Kelarutan senyawa ion dalam air merupakan salah satu sifat penting yang perlu dipahami. Senyawa ion umumnya memiliki kelarutan yang tinggi dalam air karena ion-ion penyusunnya dapat berinteraksi dengan molekul air.
Tip 5: Pahami Reaktivitas Kimia Senyawa Ion
Senyawa ion memiliki reaktivitas kimia yang tinggi karena adanya ion-ion yang berlawanan muatan. Ion-ion ini dapat bereaksi dengan zat lain untuk membentuk senyawa baru. Reaktivitas kimia ini sangat penting dalam berbagai aplikasi senyawa ion, seperti dalam produksi bahan kimia dan obat-obatan.
Kesimpulan
Memahami sifat senyawa ion sangat penting untuk menguasai konsep kimia dasar dan untuk memahami berbagai aplikasi senyawa ion dalam kehidupan sehari-hari. Dengan mengikuti tips yang telah diuraikan, Anda akan dapat memahami sifat senyawa ion dengan lebih baik dan menghargai peran pentingnya dalam berbagai bidang.
Sifat Senyawa Ion
Sifat senyawa ion, yang ditentukan oleh ikatan antara ion berlawanan muatan, memainkan peran penting dalam berbagai bidang. Titik leleh dan didihnya yang tinggi, kelarutannya dalam air, penghantaran listriknya, bentuk kristalnya yang khas, reaktivitasnya yang tinggi, dan kegunaannya yang luas menjadikannya bahan penting dalam industri, teknologi, dan biologi.
Memahami sifat senyawa ion sangat penting untuk kemajuan ilmu pengetahuan dan teknologi. Dengan terus meneliti dan mengeksplorasi sifat-sifat ini, kita dapat menemukan aplikasi baru dan inovatif untuk senyawa ion, berkontribusi pada kemajuan masyarakat dan kesejahteraan manusia.
Youtube Video:
